AIM2 단백질, 바이러스 탐지 및 염증 반응 유도 역할 밝혀져
바이러스 서열 길이에 따른 면역 반응 강도 차이 발견
면역 센서 조절 통한 새로운 감염병 치료 전략 가능성 제시
전 세계 인구의 약 67퍼센트가 흔히 감염되는 헤르페스 제1형 바이러스, 우리는 어떻게 우리의 몸이 이러한 바이러스와 싸우는지 연구진의 발견을 통해 새롭게 알 수 있게 되었다.
울산과학기술원(UNIST)의 이상준 교수팀은 성균관대, 제주대, 기초과학연구원 등과 협력하여 헤르페스 바이러스 DNA의 반복 서열이 면역 반응을 유발한다는 사실을 규명했다. 그들은 바이러스 DNA 중 티민 염기 분자인 poly(T) 서열을 집중적으로 분석하여 면역 시스템의 감지 과정을 이해하게 되었다.
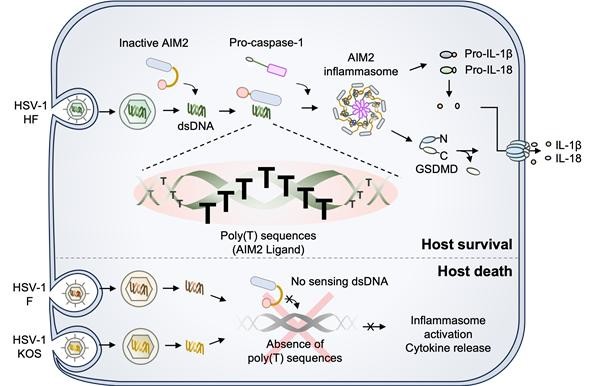 |
| ▲숙주의 면역 센서가 바이러스 DNA를 인식하는 원리. |
특히 선천 면역 센서인 AIM2의 역할이 주목받았다. AIM2는 대식세포에서 바이러스의 존재를 탐지하는 단백질로, poly(T) 서열을 인식하여 염증 반응과 감염 세포의 사멸을 유도한다.
이 연구는 이러한 반복 서열이 다양하게 존재하는 바이러스에 따라서 면역 반응 강도가 달라질 수 있음을 보여주며, 특히 서열의 길이가 길수록 강한 면역 반응을 유도한다는 것을 발견했다. 이는 새로운 바이러스 감염 치료 전략으로써의 가능성을 열어준다.
이상준 교수는 이 연구가 중증 감염병 바이러스와 관련된 면역 반응 조절법 개발에 큰 기여를 할 것이라고 말했다. 바이러스 자체를 직접 공격하는 전통적인 치료법 대신, 이번 연구는 면역 센서를 조절하는 접근이 새로운 대안으로 주목받을 수 있음을 시사한다.
새로운 맞춤형 면역 조절 신약 개발의 토대가 될 수 있을 것이란 기대가 모아지는 가운데, 이 획기적인 연구는 국제 학술지에 게재되어 전 세계의 주목을 받고 있다. 연구는 여러 기관 및 재단의 지원 아래 이루어졌으며, 감염병 치료에 새로운 방향성을 제시하고 있다.
[저작권자ⓒ 미디어시시비비. 무단전재-재배포 금지]



































![[특별 부록] 『율력융통』 원문- 명리학 박사 논문 날조를 증명한다-이상엽](/news/data/20260424/p1065543476246153_245_h2.png)
![[새 책] 『고립경제학』- 벤추 지음. 고한석 옮김.](/news/data/20260426/p1065573482406079_803_h2.png)
![<『율력융통(律曆融通)』으로 본 입춘 세수(歲首)설 연구>에 대한 공개 반론 및 질의-[18]](/news/data/20260416/p1065568659533511_239_h2.png)
![[박한표] 정치인보다 유권자가 깨어나야 한다.](/news/data/20260418/p1065570966307716_193_h2.jpg)





